COVID-19(新型コロナウイルス感染症)感染症
COVID-19(新型コロナウイルス感染症)の発⽣状況2020年3⽉1⽇時点における本ウイルス感染者数は全世界で約8万7千⼈、死亡者数は約3,000⼈となっています。
COVID-19(新型コロナウイルス感染症)の臨床的特徴
新型コロナウイルス感染症は呼吸器系の感染が主体です。ウイルスの主な感染部位により肺炎を発症すると考えられます。本ウイルスに感染した⽅全員が発症するわけではなく、無症状で経過してウイルスが排除される例も存在します
COVID-19(新型コロナウイルス感染症)の治療・予防
新型コロナウイルス感染症(COVID-19)に対し現在、有効性が証明された治療法はありません。ロピナビル/リトナビル(抗HIV薬)、アビガン(抗インフルエンザ薬)、レムデシビル(エボラ出⾎熱)が有用でないかと言われており、今後、治療薬なる可能性があります。
COVID-19(新型コロナウイルス感染症)の集団感染を防ぐためにすべきこと
集団感染が確認された場に共通する
・換気の悪い密閉空間
・人が密集している
・近距離での会話や発声が行われる
という3つの条件が同時に重なった場所(換気が悪く、人が密に集まって過ごすような空間(密閉空間・密集場所・密接場所))に集団で集まることは避けてください。
COVID-19(新型コロナウイルス感染症)の臨床的診断と検査対象
新型コロナウイルス感染症に特異的な症状や所⾒はないとされます。症状、診察所⾒および各種検査所⾒を踏まえて、まず他の感染症および発熱性疾患との鑑別が重要となります。
特に類似した症状を⽰すとされるインフルエンザや他の感染症の抗原検査等を⾏い除外診断を実施する必要があります。
新型コロナウイルス感染症
|
普通感冒(かぜ)
インフルエンザ急性胃腸炎
|
|
症状
|
発熱,呼吸器症状,倦怠感下痢,嘔吐
|
|
経過期間
|
約7⽇間持続する
悪化するときは急激に進⾏
|
3〜4⽇で軽快し始める
|
合併症
|
約2割で肺炎
|
⼊院を要する合併症は⽐較的稀
|
新型コロナウイルスの遺伝子検査の検査対象
濃厚接触歴などが無くとも、新型コロナウイルス以外の呼吸器感染症が否定されれば、検査対象になります

※日経バイオテクより引用
検査に当たっては、事前に保健所へ相談し、検査が決まれば医師が検体を採取。感染研や地方衛生研究所で検査を実施するか、臨床検査会社や一部の大学病院の協力を得て、検査を実施する流れです

※日経バイオテクより引用
検査に当たっては、事前に保健所へ相談し、検査が決まれば医師が検体を採取。感染研や地方衛生研究所で検査を実施するか、臨床検査会社や一部の大学病院の協力を得て、検査を実施する流れです
COVID-19(新型コロナウイルス感染症)のウイルス学的診断
ウイルス検査にはPCR法など核酸増幅法が⽤いられており、医療機関から疑似症として保健所に届出後、国⽴感染症研究所、地⽅衛⽣研究所、および検疫所で検査が実施されています。検査体制の拡充により、外注検査センターや⼤学でも検査が実施できる体制が整えられてきているため、さらに検査可能なケースが増えてくると思われます。
COVID-19(新型コロナウイルス感染症)の抗体検査
PCR法と比較して採血で行う抗体検査の利点として
(1)PCR 検査と比べると医療従事者の感染リスクも大幅に軽減される、
(2)PCR 検査と異なり、免疫獲得の確認や、集団免疫の把握等に適している
とされます
ヤマト科学は研究用試薬として新型コロナウイルス(SARS-CoV-2)の
IgM抗体、IgG抗体を同時に10分で検出するキットを2020年4月13日から50,000円(20カセット/1箱)で国内販売を開始しました

COVID-19(新型コロナウイルス感染症)の迅速検出キット現る

ヤマト科学は研究用試薬として新型コロナウイルス(SARS-CoV-2)の
IgM抗体、IgG抗体を同時に10分で検出するキットを2020年4月13日から50,000円(20カセット/1箱)で国内販売を開始しました

本製品は研究用みたいです
新型コロナウイルス感染症に係るPCR検査の保険適用
PCR検査「SARS-CoV-2(新型コロナウイルス)核酸検出」を3月6日から保険適用となりました。SARSコロナウイルス核酸検出450点」の4回分1,800点とされます。
※大学病院内で検査する場合など、カテゴリーB感染物質輸送を行わない場合は3回分1,350点となります
保険適用となる検査方法は以下の通りです
(1)国立感染症研究所が作成した「病原体検出マニュアル2019-nCoV」又はそれに準じた方法
(2)SARS-CoV-2の検出(COVID-19の診断又は診断の補助)を目的として薬事承認又は認証を得ているもの
が対象となります
保険適用している新型コロナウイルス(2019-nCoV)の遺伝子検査方法(RT-PCR法)
逆転写及び遺伝子増幅に1時間以上かかるもの
・LightMixRModularSARSandWuhanCoVE-gene、ロシュ・ダイアグノスティックス株式会社)
・LightMixRModularSARSandWuhanCoVN-gene(ロシュ・ダイアグノスティックス株式会社)
・LightMixRModularSARSandWuhanCoVE-gene(ロシュ・ダイアグノスティックス株式会社)
・新型コロナウイルス検出RT-qPCRキット(BGI社)
・FLUOROSEARCHTMNovelCoronavirus(SARSCoV-2)DetectionKit(医学生物学研究所)
迅速な検査方法(逆転写及び遺伝子増幅が1時間未満のもの)
・Loopamp2019-nCoV検出試薬キット(栄研化学社)
・SARS-CoV-2GeneSoCER杏林(杏林製薬)
・SmartAmp2019新型コロナウイルス検出試薬(株式会社ダナフォーム)
COVID-19(新型コロナウイルス感染症)の遺伝子検査方法の比較
国立感染症研究所の遺伝子検査方法の比較のデータがありますが
下記の試薬では90%以上の陽性一致率及び陰性一致率が認めれます
LightMixR
Modular SARS-CoV(COVID19) E-gene
|
ロシュ
|
陽性一致率 100% (10/10)
陰性一致率 100% (15/15)
|
新型コロナウイルス検出 RT-qPCR キッ ト
|
BGI 社
|
陽性一致率 100% (10/10)
陰性一致率 100% (15/15)
|
FLUOROSEARCH™
Novel Coronavirus
(SARS-CoV-2)
Detection Kit
|
医学生物学研究所
|
陽性一致率 100% (10/10)
陰性一致率 100% (15/15)
|
TaqMan
SARS-CoV-2 Assay Kit v2 (Multiplex)
|
ライフテクノロジーズ
ジャパン
|
陽性一致率 100% (10/10)
陰性一致率 100% (15/15)
|
Loopamp
2019-nCoV 検出試薬キット
|
栄研化学
|
陽性一致率 90% (9/10)
陰性一致率 100% (15/15)
|
SARS-CoV-2
GeneSoC ER 杏林
|
杏林製薬
|
陽性一致率 90% (9/10)
陰性一致率 100% (15/15)
|
OVID-19(新型コロナウイルス感染症)の遺伝子検査で注意すべき点
遺伝子検査(RT-PCR法)とは、鼻咽頭拭い液(鼻から綿棒を挿入し鼻中腔の近くでこすり取った検査材料)などに微量に含まれる病原体特有のゲノム配列だけをPCR法と呼ばれる手法で増幅し、病原体の有無を調べる検査で核酸の抽出、増幅。抽出が肝となります
PCR検査はウイルスゲノムを検出するという原理から,感度は低く,特異度が⾼いと考えられます.新型コロナウイルス感染症患者であるにもかかわらず,誤って陰性となり⾒逃される患者が⼀定数出ます.この場合,偽陰性となった患者が陰性結果に安⼼して外出する等して,感染が拡⼤するおそれがあります.検査件数が増加すれば,偽陰性で⾒逃される新型コロナウイルス感染者も増加し,感染拡⼤のリスクも⾼くなります.
インフルエンザ迅速検査が陰性であっても,新型コロナウイルス感染症の疑いが直ちに強くなるとは⾔えません.インフルエンザ検査が陽性の場合,⾼確率でインフルエンザと診断できますが,インフルエンザと新型コロナウイルスが重複感染していることがありえるため新型コロナウイルス感染症を否定できません.
海外におけるCOVID-19(新型コロナウイルス感染症)の検査事情
米国
公開された新型コロナウイルスのゲノム配列情報を基に米疾病対策センター(CDC)が自家調整の遺伝子検査(リアルタイムRT-PCR法)を確立してます。自家調整の遺伝子検査に必要な最低限の試薬(プライマーとプローブ、ポジティブコントロール)を診断パネルとしてキット化。
2月4日付で、同診断パネルについて米食品医薬品局(FDA)から緊急使用許可(Emergency Use Authorization:EUA)を取得した。
1セットの診断パネルで700例から800例の遺伝子検査が可能だそうです
中国や韓国
Roche社などの研究用試薬を用いた遺伝子検査が実施されていおり韓国では正しく検査が実施できるか、検証を行った上で、順次、研究用試薬による遺伝子検査を行う体制を整えているらしいです
本邦との比較
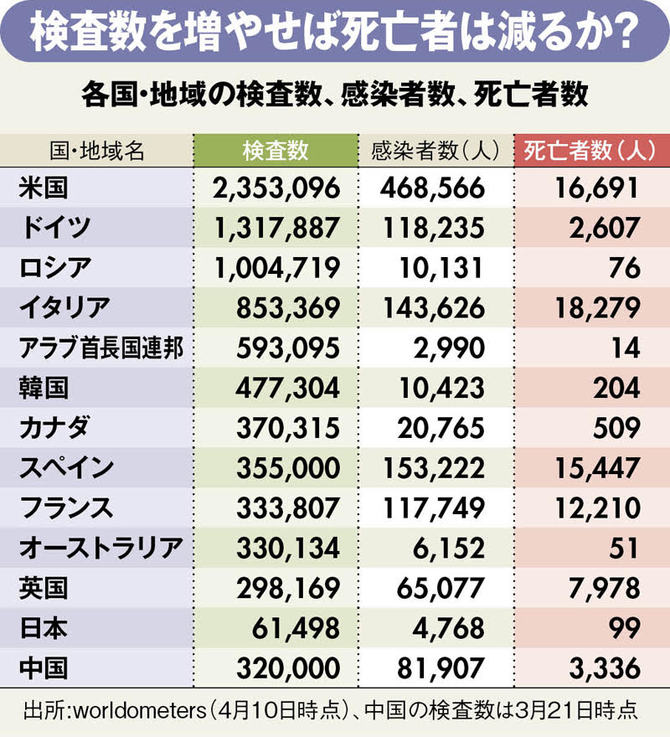
※ダイヤモンドオンラインより引用
韓国やイタリアは、当初から大量の検査件数をこなした結果、軽症者が病院に押し寄せて医療キャパシティーがパンクしたという経緯がありました。
各国の検査数、感染者数、死亡者数の比較ですが他の国でも検査数と死亡者数はあまり相関性がないようです
国内の遺伝子検査事情
国立研究開発法人 日本医療研究開発機構が行った国内における遺伝子関連検査の実施状況(遺伝子関連検査の実施状況等に関するアンケート調査)では
遺伝子検査は病院・診療所では外部委託が多く病院ではは75.4%が検査センターへ委託しております
また検査センターの41.8%が国内の外部機関に再外注しております
病原体遺伝子検査に関して言えば86施設、260,007件を機関内で実施しているにすぎません
遺伝子検査では
・検体中の遺伝子(病原体・DNA・RNA・タンパク等)の取扱い
・検体の処理
・遺伝子検査技術
といったスキルが必要となりますが、遺伝子検査を行っている施設と言えば、保健所や検査センター、大手医療機関などで行われており
殆どの技師の方は技師学校や大学院でしか扱っただけという方が自分の周りではほとんどを占めます
検査の拡大に伴って生じる「検査の質」という新たな懸念もあります
「検体からRNAを抽出する工程などの施設間差の指摘や
また2018年度12月の医療法改正にもありましたが、遺伝子検査の精度管理や品質管理も問題もあり検査の質の担保は避けては通れない課題なります
COVID-19(新型コロナウイルス感染症)遺伝子検査が後手に回った理由
新型コロナウイルスの検査体制の増強がここまで後手後手になっているのか?新型コロナウイルスによる感染症(COVID-19)は新しい感染症(新興感染症)かつ未知の病原体が原因であるため基本体外診断薬はしません
このため新興感染症に対して公開された病原体のゲノム配列情報に基づい国立感染症研究所(感染研)が、必要な試薬や装置を組み合わせ、
自家調整(home-brew)の遺伝子検査(RT-PCR法)を確立します
感染研が主導して、全国に約八十数カ所ある傘下の地方衛生研究所でも感染拡大に備え、同様の自家調整の遺伝子検査ができるよう全国で検査体制を整えております。
このため地方衛生研究所で体制が整うまでには、時間がかかります。
感染研を中心とした検査体制では、新型コロナウイルスの遺伝子検査のキャパシティーは、2月12日時点で1日最大300件程度と報告されております
遺伝子検査を大規模に行っているわけではなく感染研の人員には限りがありますし
感染研が確立した自家調整の遺伝子検査に必要な試薬も大量に製造・流通している訳ではありません
引用
・病原体検出マニュアル2019-nCoVVer.2.8
・臨床検体を用いた評価結果が取得された2019-nCoV遺伝子検査方法について
・国内における遺伝子関連検査の実施状況
(遺伝子関連検査の実施状況等に関するアンケート調査)
・日経バイオテク
・ダイヤモンドオンライン
・国内における遺伝子関連検査の実施状況
(遺伝子関連検査の実施状況等に関するアンケート調査)
・日経バイオテク
・ダイヤモンドオンライン










0 件のコメント:
コメントを投稿